Revista Colombiana de
Tecnologías de Avanzada
Tecnologías de Avanzada
Recibido: 18 de abril de 2022
Aceptado: 15 junio de 2022
Aceptado: 15 junio de 2022
IDENTIFICACIÓN AUTOMÁTICA DE CÁNCER DE PIEL APLICANDO MACHINE LEARNING
AUTOMATIC IDENTIFICATION OF SKIN CANCER USING MACHINE LEARNING
 MSc. Anderson Smith Flórez Fuentes*,
MSc. Anderson Smith Flórez Fuentes*,
 PhD. Rafael Guzmán Cabrera*,
PhD. Rafael Guzmán Cabrera*,
 PhD. Everardo Vargas Rodríguez*
PhD. Everardo Vargas Rodríguez*
* Universidad de Guanajuato, Doctorado en Ciencias de Ingeniería.
Tel.: +52-7295416779, +52 4641239321
E-mail: {as.florezfuentes, guzmanc, evr}@ugto.mx
AUTOMATIC IDENTIFICATION OF SKIN CANCER USING MACHINE LEARNING
 MSc. Anderson Smith Flórez Fuentes*,
MSc. Anderson Smith Flórez Fuentes*,
 PhD. Rafael Guzmán Cabrera*,
PhD. Rafael Guzmán Cabrera*,
 PhD. Everardo Vargas Rodríguez*
PhD. Everardo Vargas Rodríguez*
* Universidad de Guanajuato, Doctorado en Ciencias de Ingeniería.
Tel.: +52-7295416779, +52 4641239321
E-mail: {as.florezfuentes, guzmanc, evr}@ugto.mx
Cómo citar: Florez Fuentes, A. S., Guzmán Cabrera, R., & Vargas Rodriguez, E. (2022).
IDENTIFICACIÓN AUTOMÁTICA DE CÁNCER DE PIEL APLICANDO MACHINE LEARNING. REVISTA COLOMBIANA DE TECNOLOGIAS DE
AVANZADA (RCTA), 2(40), 1-6. https://doi.org/10.24054/rcta.v2i40.2350
Derechos de autor 2022 Revista Colombiana de Tecnologías de Avanzada (RCTA).
Esta obra está bajo una licencia internacional
Creative Commons
Atribución-NoComercial 4.0.


Resumen: En la actualidad la implementación del machine learning en la medicina,
especial en la oncología, se ha convertido en una herramienta clave para la detección de malformaciones,
infecciones, problemas cardiacos, cáncer, entre otros, anomalías del cuerpo humano qué al aplicar
aprendizaje
automático, estos procesos se convierten en herramientas que fortalecen el diagnóstico médico. En este
trabajo se
presenta una revisión de la literatura y los resultados obtenidos de una implementación en Python para
llevar a cabo
la clasificación de imágenes médicas con presencia de cáncer de piel. Se utilizaron cuatro métodos de
aprendizaje distintos:
máquinas de vectores de soporte, vecinos más cercanos, redes neuronales y árboles de decisión. Se utilizó la
base de datos HAM10000,
la cual contiene imágenes médicas manualmente etiquetadas, lo que asegura que el proceso de entrenamiento
sea efectivo.
En la implementación de una muestra balanceada, la que permite demostrar la eficiencia de la implementación
realizada en
la identificación del cáncer de piel, esta implementación tiene una gran variabilidad en los resultados,
alcanzando
valores cercanos al 100% de precisión en algunos casos.
Palabras clave: Cáncer de piel, Machine learning, procesamiento, data.
Abstract: Currently the implementation of machine learning in medicine, especially in oncology, has become a key tool for the detection of malformations, infections, heart problems, cancer, among others, anomalies of the human body that by applying machine learning, these processes become tools that strengthen the medical diagnosis. This work presents a literature review and the implementation with Python to analyze the behavior of the implemented data, performing an execution for four types of models such as support vector machine, k-nearest neighbor, Neural Network and Decision Tree, these models are applied to the HAM10000 data, which contains manually labeled medical images, which ensures that the delivery process is effective. In the implementation of a balanced sample, which allows to demonstrate the efficiency of the implementation of machine learning in the identification of skin cancer, this implementation has a great variability in the results, reaching values up to 100% accuracy in the implementation.
Keywords: Skin cancer, Machine learning, processing, data.
Al hablar de ML, es indispensable también agregar los conceptos de Aprendizaje Supervisado y No Supervisado, donde (
Por otro lado, el ML también contribuye con el Deep Learning (DL) o aprendizaje profundo, el cual
La inteligencia artificial y su aplicación en múltiples áreas es una realidad, si analizamos profundamente, se puede encontrar inteligencia artificial, en dispositivos o aplicaciones que utilizamos día a día, como teléfonos móviles, lavadoras, televisores, neveras, parlantes entre otros, y si bien este uso se da en este tipo de dispositivos, de igual manera se da en muchas otras áreas, como: construcción, entidades financieras, casa de apuestas o salud, por mencionar algunos. En años recientes se ha hecho uso de la inteligencia artificial en diversas aplicaciones dada su versatilidad y aplicada correctamente puede generar diagnósticos a enfermedades entre los que destacan: síntomas
Según la Organización Mundial de la Salud
En este procedimiento se realiza también una implementación con python para poder analizar el comportamiento de las predicciones en cada uno de los modelos, como K-Nearest-Neighbor (kNN), Support vector machine (SVM), Decisión Tree (Tree), Neural Network, modelos que permiten realizar un análisis del comportamiento del sistema ante las imágenes manualmente etiquetadas que se implementan como muestra, para este proceso se tomó una muestra por cada uno de los 7 tipos de cáncer de piel que trae la Data analizada para este trabajo, como pauta inicial.
De igual forma se realiza la implementación de la data HAM10000
En el trabajo presentado por
Dentro de la clasificación de las anomalías de la piel
Por otro lado, y teniendo en cuenta el aumento drástico en la tasa de fatalidades por cancel de piel dadas las variedades de la sintomatología, confirma que la detección temprana en la etapa prematura es necesaria para prevenir la propagación del cáncer. Por ejemplo, Krishna Monika et al.
En este proceso se aplican kNN, SVM, TREE, Neural Network, cuyos resultados de predicción se complementan con el resultado del análisis de AUC, AC y predicted el modelo de la fig.3, para poder analizar correctamente se realiza para la implementación de las 200 y 400 imágenes de entrenamiento (train) y 30 y 60 imágenes de prueba (test), obteniendo buenos resultados pese a resultados tienen una gran variación, obteniendo los mejores resultados de manera inicial al aplicar el modelo de maquina de soporte vectorial SVM, en donde se puede visualizar en la fig 4, el resultado más alto de predicción lo tiene el melanoma (mel).
En este procedimiento se encuentra en la ejecución del segundo grupo de imágenes correspondientes a las 400 imágenes un mayor desempeño en el SVN, arrojando predicciones de hasta el 100% en la ejecución de test and score, para el modelo de la máquina de soporte vectorial SVM. Si bien se presentan resultados de 100% en la ejecución, estos resultados varían acorde a las muestras implementadas y el tipo de muestra seleccionada, esto permite ajustar las fórmulas para encontrar una precisión en constante mejora, y que la variación entre las muestras no afecte los altos porcentajes de predicción calculados.
Esta implementación permitió poder tener de manera sólida una descripción de apoyo a la aplicación de herramientas para verificar la predicción que se genera en la implementación de modelos de inteligencia artificial, generando predicciones que permiten clasificar con un alto grado de precisión, que permita detectar si, las muestras escogidas hacen parte de un cáncer de piel o no, de esta forma brindarle al dermatólogo o al oncólogo tener un primer análisis de las muestras analizadas.
Al-masni, M. A., Kim, D., & Kim, T. (2020). Computer Methods and Programs in Biomedicine Multiple skin lesions diagnostics via integrated deep convolutional networks for segmentation and classification. Computer Methods and Programs in Biomedicine, 190, 105351. https://doi.org/10.1016/j.cmpb.2020.105351
Daneshjou, R., He, B., Ouyang, D., & Zou, J. Y. (2021). How to evaluate deep learning for cancer diagnostics – factors and recommendations. Biochimica et Biophysica Acta (BBA) - Reviews on Cancer, 1875(2), 188515. https://doi.org/10.1016/J.BBCAN.2021.188515
Deng, L., & Yu, D. (2019). Deep Learning Methods and Applications. SpringerBriefs in Computer Science, 31–42. https://doi.org/10.1007/978-981-13-3459-7_3
Dorado-Díaz, P. I., Sampedro-Gómez, J., Vicente-Palacios, V., & Sánchez, P. L. (2019). Applications of Artificial Intelligence in Cardiology. The Future is Already Here. In Revista Espanola de Cardiologia (Vol. 72, Issue 12, pp. 1065–1075). Elsevier Doyma. https://doi.org/10.1016/j.recesp.2019.05.016
Fontecha Pardo, N. A., Quiroga Sarmiento, J. S., nicolas.fontechap@campusucc.edu.co, & juan.quirogas@campusucc.edu.co. (2020). Implementación de algoritmos de inteligencia artificial enfocados en el análisis de los trastornos del estado de ánimo para prevenir futuros suicidios por medio de la red social Facebook. Aprendeia. (22 de 11 de 2020). Obtenido de Https://Aprendeia.Com/Naive-Bayes-Teoria-Machine-Learning/.
Garay, N., Abascal, J., & Gardeazabal, L. (2002). Mediación emocional aplicada en sistemas de comunicación aumentativa y alternativa. Inteligencia Artificial, 6(16). https://doi.org/10.4114/ia.v6i16.743
Gómez Rivas, J., Toribio Vázquez, C., Ballesteros Ruiz, C., Taratkin, M., Marenco, J. L., Cacciamani, G. E., Checcucci, E., Okhunov, Z., Enikeev, D., Esperto, F., Grossmann, R., Somani, B., & Veneziano, D. (2021). Inteligencia artificial y simulación en urología. Actas Urológicas Españolas. https://doi.org/10.1016/J.ACURO.2020.10.012
Han, S. S., Park, I., Chang, S. E., Lim, W., & Kim, M. S. (2020). Augmented Intelligence Dermatology : Deep Neural Networks Empower Medical Professionals in Diagnosing Skin Cancer and Predicting Treatment Options for 134 Skin Disorders. Journal of Investigative Dermatology, 140(9), 1753–1761. https://doi.org/10.1016/j.jid.2020.01.019
Hekler, A., Utikal, J. S., Enk, A. H., Hauschild, A., Weichenthal, M., Maron, R. C., Berking, C., Haferkamp, S., Klode, J., Schadendorf, D., Schilling, B., Holland-Letz, T., Izar, B., von Kalle, C., Fröhling, S., Brinker, T. J., Schmitt, L., Peitsch, W. K., Hoffmann, F., … Thiem, A. (2019). Superior skin cancer classification by the combination of human and artificial intelligence. European Journal of Cancer, 120, 114–121. https://doi.org/10.1016/J.EJCA.2019.07.019
Hernández, J. C. (2020). PROBLEMAS ÉTICO-JURÍDICOS DE LAS DECISIONES ALGORÍTMICAS Y EL BIG DATA * Joslay Polanco Medina.
Jofre, M., & Abeldaño, A. (2021). Artificial intelligence: Will replace the dermatologist making diagnoses? Piel, 36(5), 331–335. https://doi.org/10.1016/j.piel.2020.06.003
Koh, J., Yoon, Y., Kim, S., Han, K., & Kim, E. K. (2021). Deep Learning for the Detection of Breast Cancers on Chest Computed Tomography. Clinical Breast Cancer. https://doi.org/10.1016/J.CLBC.2021.04.015
Krishna Monika, M., Arun Vignesh, N., Usha Kumari, C., Kumar, M. N. V. S. S., & Laxmi Lydia, E. (2020). Skin cancer detection and classification using machine learning. Materials Today: Proceedings, 33, 4266–4270. https://doi.org/10.1016/J.MATPR.2020.07.366
Leiva Vazquez, M., Gonzalez Benitez, N., Hechavarria Hernandez, J., Rivero Peña, Y., & Daher Nader, J. E. (2018). El diagnóstico de enfermedades desde el Análisis Inteligente de los Datos.
Maisueche Cuadrado, A. (2019). Utilización Del Machine Learning En La Industria 4.0.
McClendon, L., & Meghanathan, N. (2015). Using Machine Learning Algorithms to Analyze Crime Data. Machine Learning and Applications: An International Journal, 2(1), 1–12. https://doi.org/10.5121/mlaij.2015.2101
Mitchel, T. M. (2017). Machine Learning. In Proceedings of the International Conference on Document Analysis and Recognition, ICDAR. https://doi.org/10.1109/ICDAR.2019.00014
Organización Mundial de La Salud, O. (2021). Cáncer. WHO.
P, T., C, R., & H, K. (2018). The HAM10000 dataset, a large collection of multi-source dermatoscopic images of common pigmented skin lesions. Scientific Data, 5. https://doi.org/10.1038/SDATA.2018.161
Russel, S., & Norvig, P. (2010). Artificial intelligence, A Modern Approach. In 2010 The 2nd International Conference on Computer and Automation Engineering, ICCAE 2010 (Vol. 4). https://doi.org/10.1109/ICCAE.2010.5451578
Saravanan, S., Heshma, B., Shanofer, A. V. A., & Vanithamani, R. (2020). Skin cancer detection using dermoscope images. Materials Today: Proceedings, xxxx. https://doi.org/10.1016/j.matpr.2020.08.388
Yan, T., Zhang, L., & Peng, C. (2019). Intelligent skin cancer diagnosis using improved particle swarm optimization and deep learning models. Applied Soft Computing Journal, 84, 105725. https://doi.org/10.1016/j.asoc.2019.105725
Yin, S., Peng, Q., Li, H., Zhang, Z., You, X., Fischer, K., Furth, S. L., Fan, Y., & Tasian, G. E. (2020). Multi-instance Deep Learning of Ultrasound Imaging Data for Pattern Classification of Congenital Abnormalities of the Kidney and Urinary Tract in Children. Urology, 142, 183–189. https://doi.org/10.1016/J.UROLOGY.2020.05.019
Palabras clave: Cáncer de piel, Machine learning, procesamiento, data.
Abstract: Currently the implementation of machine learning in medicine, especially in oncology, has become a key tool for the detection of malformations, infections, heart problems, cancer, among others, anomalies of the human body that by applying machine learning, these processes become tools that strengthen the medical diagnosis. This work presents a literature review and the implementation with Python to analyze the behavior of the implemented data, performing an execution for four types of models such as support vector machine, k-nearest neighbor, Neural Network and Decision Tree, these models are applied to the HAM10000 data, which contains manually labeled medical images, which ensures that the delivery process is effective. In the implementation of a balanced sample, which allows to demonstrate the efficiency of the implementation of machine learning in the identification of skin cancer, this implementation has a great variability in the results, reaching values up to 100% accuracy in the implementation.
Keywords: Skin cancer, Machine learning, processing, data.
1. INTRODUCCIÓN
El término Machine Learning (ML) fue acuñado por primera vez en 1959 por Arthur Samuel (Hernández, 2020
)
. Su objetivo es desarrollar algoritmos que permitan a los sistemas de cómputo tomar decisiones y aprender
de los resultados; es decir,
los sistemas serían capaces de aprender a realizar una tarea sin haber sido provisto explícitamente con la
programación requerida
(PROBLEMAS ÉTICO-JURÍDICOS DE LAS DECISIONES
ALGORÍTMICAS Y EL BIG DATA * Joslay Polanco Medina.
Dorado-Díaz et al., 2019
;
Applications of Artificial
Intelligence in Cardiology. The Future is Already Here. In Revista Espanola de Cardiologia (Vol. 72,
Issue 12, pp. 1065–1075). Elsevier Doyma. https://doi.org/10.1016/j.recesp.2019.05.016.
McClendon & Meghanathan, 2015
).
De igual manera Using Machine Learning
Algorithms to Analyze Crime Data. Machine Learning and Applications: An International Journal, 2(1),
1–12. https://doi.org/10.5121/mlaij.2015.2101.
(Mitchel, 2017)
define “Un programa de computadora se dice que aprende desde la experiencia E con respecto a alguna
clase de tareas T y medida de performance P, si mejora su performance con las tareas en T, con respecto a la
medida P,
basado en la experiencia E”, expresando de manera clara y puntual como se aprende desde la experiencia.
Machine Learning. In
Proceedings of the International Conference on Document Analysis and Recognition, ICDAR. https://doi.org/10.1109/ICDAR.2019.00014.
Al hablar de ML, es indispensable también agregar los conceptos de Aprendizaje Supervisado y No Supervisado, donde (
Maisueche Cuadrado, 2019
;Utilización Del Machine Learning En
La Industria 4.0.
Russel & Norvig, 2010
)
describen de manera sencilla el aprendizaje supervisado como, el agente que observa pares
de datos de entrada y salida a modo de ejemplo para aprender una función que modele la salida según la
entrada, así como también
amplían el concepto sobre la resolución de problemas por medio de los algoritmos de regresión y de
clasificación. De igual forma
describen el aprendizaje no supervisado como el agente encargado de detectar patrones existentes en los
datos de entrada sin
necesidad de observar la salida. Es decir, en el aprendizaje supervisado se requieren instancias etiquetadas
como entrenamiento,
que son usadas por el sistema automático para aprender, mientras que en el aprendizaje no supervisado no se
requiere de
estas instancias.
Artificial intelligence, A Modern
Approach. In 2010 The 2nd International Conference on Computer and Automation Engineering, ICCAE
2010 (Vol. 4). https://doi.org/10.1109/ICCAE.2010.5451578.
Por otro lado, el ML también contribuye con el Deep Learning (DL) o aprendizaje profundo, el cual
(Deng & Yu, 2019)
describen como, una clase de técnicas de aprendizaje automático que explotan muchas capas de procesamiento
de información no lineal para la extracción
y transformación de características supervisadas o no supervisadas, para el análisis y clasificación de
patrones. De igual forma amplían,
el DL que trata de aprender múltiples niveles de representación y abstracción que ayudan a dar sentido a
datos como imágenes, sonido y
texto. También refiere el DL como una clase bastante amplia de técnicas y arquitecturas de ML, con el sello
distintivo de utilizar muchas
capas de procesamiento de información no lineal que son de naturaleza jerárquica, el cual se puede
cómodamente clasificar en: Redes
profundas para el aprendizaje generativo o no supervisado, Redes profundas para el aprendizaje supervisado y
Redes profundas híbridas.
Deep Learning Methods and Applications.
SpringerBriefs in Computer Science, 31–42. https://doi.org/10.1007/978-981-13-3459-7_3.
La inteligencia artificial y su aplicación en múltiples áreas es una realidad, si analizamos profundamente, se puede encontrar inteligencia artificial, en dispositivos o aplicaciones que utilizamos día a día, como teléfonos móviles, lavadoras, televisores, neveras, parlantes entre otros, y si bien este uso se da en este tipo de dispositivos, de igual manera se da en muchas otras áreas, como: construcción, entidades financieras, casa de apuestas o salud, por mencionar algunos. En años recientes se ha hecho uso de la inteligencia artificial en diversas aplicaciones dada su versatilidad y aplicada correctamente puede generar diagnósticos a enfermedades entre los que destacan: síntomas
(Leiva Vazquez et al., 2018)
,
estados de ánimo
El diagnóstico de enfermedades desde el Análisis Inteligente de los Datos.
(Garay et al., 2002)
,
prevención de suicidios por medio de análisis a las redes sociales
Mediación emocional
aplicada en sistemas de comunicación aumentativa y alternativa. Inteligencia Artificial, 6(16). https://doi.org/10.4114/ia.v6i16.743.
(Fontecha Pardo et al., 2020)
,
entre muchas otras aplicaciones que se le puede dar a
la inteligencia artificial. En este trabajo se presenta una breve revisión de artículos relacionados con el
procesamiento de imágenes
aplicado en el diagnóstico, tratamiento y seguimiento del cáncer de piel.
Implementación de algoritmos de
inteligencia artificial enfocados en el análisis de los trastornos del estado de ánimo para prevenir
futuros suicidios por medio de la red social Facebook. Aprendeia. (22 de 11 de 2020). Obtenido de
Https://Aprendeia.Com/Naive-Bayes-Teoria-Machine-Learning/.
(Jofre & Abeldaño, 2021)
plantean como hipótesis la posibilidad de que la inteligencia artificial reemplazará al dermatólogo para
hacer
diagnósticos, aunque la idea no es absurda ni prematura, dado el gran avance que se tiene, los grandes
bancos de datos de imágenes
capturadas, los diagnósticos ya realizados sobre cada una de las imágenes por especialistas, y unido a
estos, la gran evolución que
tiene la inteligencia artificial como el caso que plantea Gómez Rivas
Artificial intelligence: Will replace
the dermatologist making diagnoses? Piel, 36(5), 331–335. https://doi.org/10.1016/j.piel.2020.06.003.
(Gómez Rivas et al., 2021)
en donde hace mención que el entrenamiento quirúrgico ha evolucionado gracias al diseño de aplicaciones que
permiten evitar complicaciones y riesgos para
el paciente al facilitar no solo la detección temprana, si no, además, la evolución de la enfermedad en el
tiempo. Anudado a esto
y de manera puntual el DL sobre el campo de la medicina, hace que no solo los diagnósticos dermatológicos
tengan alto grado de
certeza, sino también la detección de múltiples enfermedades, como el cáncer de mama (Daneshjou et al.,
2021; Koh et al., 2021),
depresiones (Abdul Hamid et al., 2021), enfermedades de vías urinarias
Inteligencia artificial y
simulación en urología. Actas Urológicas Españolas. https://doi.org/10.1016/J.ACURO.2020.10.012.
(Yin et al., 2020)
, entre otras, que pueden ser diagnosticadas
de manera eficiente, por sistemas inteligentes.
Multi-instance Deep Learning of Ultrasound
Imaging Data for Pattern Classification of Congenital Abnormalities of the Kidney and Urinary Tract
in Children. Urology, 142, 183–189. https://doi.org/10.1016/J.UROLOGY.2020.05.019.
Según la Organización Mundial de la Salud
(Organización Mundial de La Salud, 2021)
el cáncer es la principal causa de muertes en el mundo,
llegando solo en el 2020 a casi 10 millones de muertos, siendo el cáncer pulmonar con 1.8 millones de casos
registradas durante el
2020, por otro lado el número de casos registrados también es alto, por ejemplo se presentan en el cáncer de
mama, con un total de
2.26 millones de casos registrados durante el 2020, seguidos por los cáncer de pulmón, colorrectal, de
próstata, de piel y gástrico,
de manera puntual el cáncer de piel (no melanoma), alcanzo los 1.20 millones de casos durante este año, es
por ende que, al igual que
todos los casos de cáncer, es necesario realizar esfuerzos desarrollando aplicaciones que permitan una
detección temprana y facilitar
una atención adecuada y oportuna.
Cáncer. WHO.
En este procedimiento se realiza también una implementación con python para poder analizar el comportamiento de las predicciones en cada uno de los modelos, como K-Nearest-Neighbor (kNN), Support vector machine (SVM), Decisión Tree (Tree), Neural Network, modelos que permiten realizar un análisis del comportamiento del sistema ante las imágenes manualmente etiquetadas que se implementan como muestra, para este proceso se tomó una muestra por cada uno de los 7 tipos de cáncer de piel que trae la Data analizada para este trabajo, como pauta inicial.
2. METODOLOGÍA
Para la construcción de este documento de revisión, se realizaron búsquedas en bases de datos de información, con las palabras skin cáncer y cáncer de piel, descartando aquellos resultados que no abarquen estas palabras desde su resultado o que su temática principal no sean los de interés.De igual forma se realiza la implementación de la data HAM10000
(P et al., 2018)
, que consta de 10015 imágenes médicas con
presencia de cáncer de piel, manualmente etiquetadas y clasificadas por expertos acordes al tipo de cáncer,
al ser esta base de
datos una colección estándar y disponible de manera gratuita, permite a los investigadores realizar la
comparación de resultados y
metodologías. Para este experimento se tienen en cuenta los tipos de cáncer que contienen entre 230 imágenes
y 460, se toman 200
imágenes de train y 30 imágenes de test, en el segundo grupo se toman 400 imágenes de train y 60 imágenes de
test, para poder analizar el comportamiento de los modelos implementados y verificar la efectividad del
entrenamiento en un mayor número de imágenes de train.
The HAM10000 dataset, a large collection of
multi-source dermatoscopic images of common pigmented skin lesions. Scientific Data, 5. https://doi.org/10.1038/SDATA.2018.161.
3. CÁNCER DE PIEL E INTELIGENCIA ARTIFICIAL
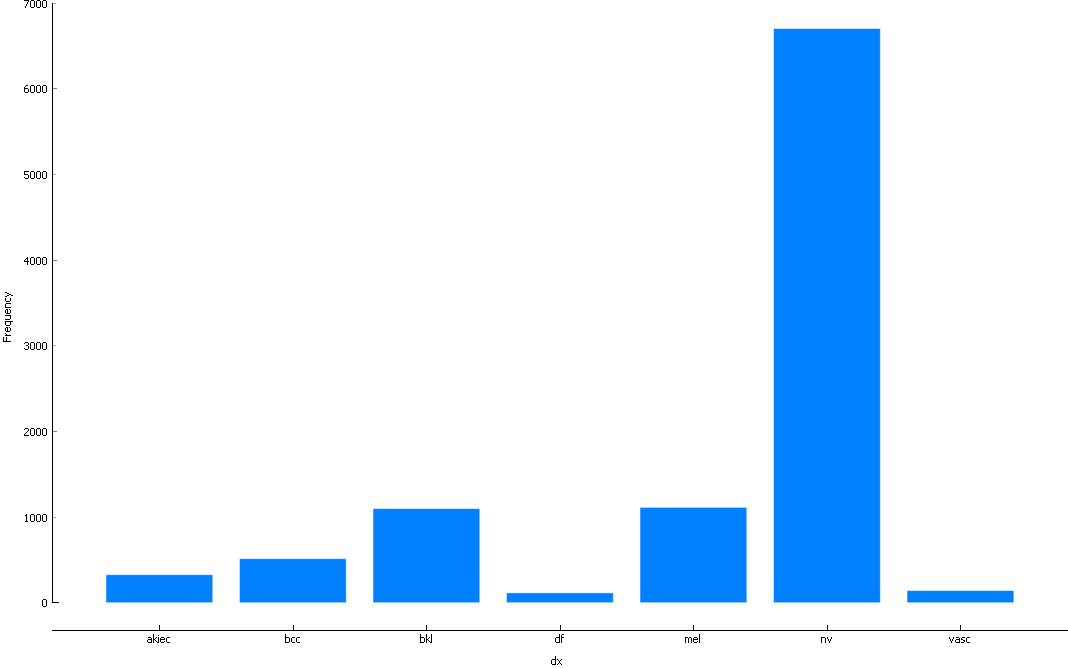
El presente trabajo se centra en analizar el comportamiento de los siguientes siete tipos de cáncer de piel: Melanocytic nevi (nv), Melanoma (mel), Benign keratosis-like lesions (bkl), Basal cell carcinoma (bcc), Actinic keratoses (akiec), Vascular lesions (vas), Dermatofibroma (df) en estos tipos de cáncer se tiene una muestra de 10000 (P et al., 2018) imágenes dermatológicas manualmente etiquetadas, las cuales se encuentran clasificada como se relacionan en la Fig 1., es de aclarar que el número de imágenes que no se tiene en cuenta en este ejercicio es considerable, este procedimiento se realiza para verificar la efectividad del entrenamiento utilizando cantidad imágenes equivalentes tanto para los train como los test.
Fig. 1 Muestra de imágenes dermatológicas
Fuente: propia
Tomando como base la cantidad de se limitó un poco más la búsqueda realizada para obtener documentos de
calidad,
adicional de poder realizar las mediciones efectivas de cuáles son los estudios realizados sobre el cáncer
de piel y
cuál ha sido la efectividad de la implementación de los sistemas inteligentes. Es por esto, que se realiza
de manera
inicial una revisión que nos permite conocer cuáles son los avances del estudio de la detección del cáncer
de piel.
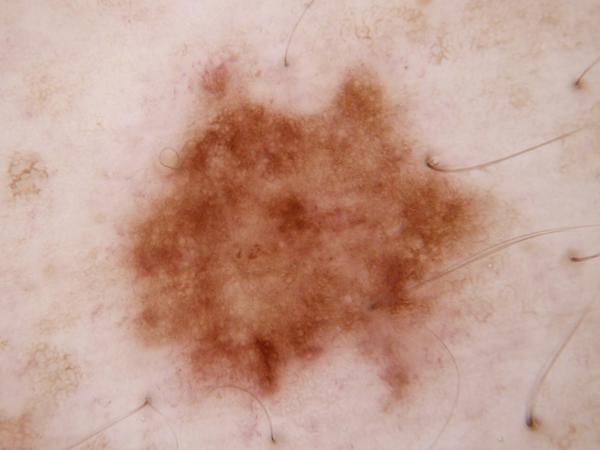
Con la finalidad de mostrar la complejidad de la tarea de clasificar las imágenes, en la Fig 2 se muestra
una imagen
de una base de datos de imágenes de cáncer de piel estándar.
Fuente: propia

Fig. 2. Cáncer de piel tipo Melanocytic nevi(nv)
fuente: https://www.kaggle.com/snginh/skinclassification-ham10k-project1
fuente: https://www.kaggle.com/snginh/skinclassification-ham10k-project1
3.1 Implementación de Sistemas Inteligentes
(Yan et al., 2019)
realiza la evaluación de dos conjuntos de lesiones cutáneas, Edimburgo Investigación e Innovación
(Dermofit) y el Servicio de Dermatología del Hospital Pedro Hispano (PH2), principalmente se centra en
realizar de manera
precisa en la extracción de características, implementando diferentes métodos como el GLRLM, LBP y HOG, esto
le permite realiza
primeramente una clasificación de lesiones benignas y malignas, implementa grupos pequeños de entrenamiento
y control, para poder
clasificar las lesiones cutáneas, en este proceso implementan clasificadores de conjuntos basados en kNN y
SVM y un modelo basado
en redes neuronales convolucionales (convolutional neural network CNN), además de la implementación de
algoritmos de búsqueda y la
implementación de unos algoritmos de optimización de enjambre de partículas (Particle Swarm Optimization,
PSO)
Intelligent skin cancer diagnosis using
improved particle swarm optimization and deep learning models. Applied Soft Computing Journal, 84,
105725. https://doi.org/10.1016/j.asoc.2019.105725.
(Hekler et al., 2019)
presentan un trabajo integrado entre la inteligencia artificial y la inteligencia humana, realizando de
manera conjunta, para ello utiliza 11,444 imágenes dermatoscópicas, que se dividieron en cinco categorías de
diagnóstico,
se utilizaron técnicas novedosas de aprendizaje profundo para entrenar a una sola CNN. Luego, 112
dermatólogos de 13 hospitales
universitarios alemanes y la CNN entrenada clasificaron de forma independiente un conjunto de 300 lesiones
cutáneas verificadas
por biopsia en cinco clases. Teniendo en cuenta la certeza de las decisiones, los dos diagnósticos
determinados de forma
independiente se combinaron en un nuevo clasificador con la ayuda de un método de aumento de gradiente. El
criterio de
valoración principal del estudio fue la clasificación correcta de las imágenes en cinco categorías
designadas, mientras que
el criterio de valoración secundario fue la clasificación correcta de las lesiones como benignas o malignas
(clasificación
binaria).
Superior skin cancer classification by
the combination of human and artificial intelligence. European Journal of Cancer, 120, 114–121. https://doi.org/10.1016/J.EJCA.2019.07.019.
En el trabajo presentado por
(Han et al., 2020)
muestran el alto rendimiento de los algoritmos de aprendizaje profundo, realizan
un análisis de 220680 imágenes de 174 trastornos de piel, divididas en 120780 imágenes en la data ASAN,
normal posee 48271 imágenes,
MED-NODE con 170, Web cuenta con 51459, SNU con 2201 y Edinburgh la cual consta 1300 imágenes y la data SNU
que consta de 2201 imágenes;
134 trastornos. Dicho algoritmo les permite predecir con precisión la malignidad, para así poder ayudar a
decidir qué tipo de tratamiento
que se puede implementar. También muestran como los clasificadores basados en aprendizaje automático superan
a los expertos humanos en el
diagnóstico de lesiones cutáneas pigmentadas tomadas desde la dermatoscopia.
Augmented Intelligence Dermatology: Deep
Neural Networks Empower Medical Professionals in Diagnosing Skin Cancer and Predicting Treatment
Options for 134 Skin Disorders. Journal of Investigative Dermatology, 140(9), 1753–1761. https://doi.org/10.1016/j.jid.2020.01.019.
Dentro de la clasificación de las anomalías de la piel
(Saravanan et al., 2020)
describe como el crecimiento anormal de piel y
la alta exposición del sol es una de las principales causas de cáncer de piel, así como también expresa que
un tratamiento efectivo
temprano es la mejor forma de curar este cáncer. El método que propusieron utiliza el módulo de desarrollo
de visión en LabVIEW para
procesar imágenes de dermoscopio. Los pasos de preprocesamiento, como el filtrado de la mediana y el
estiramiento del contraste, se
realizan para eliminar el ruido y mejorar la imagen. Adoptaron una segmentación basada en umbrales para
segmentar el área afectada.
Skin cancer detection using
dermoscope images. Materials Today: Proceedings, xxxx. https://doi.org/10.1016/j.matpr.2020.08.388.
(Al-masni et al., 2020)
realiza la evaluación de 4 clasificadores conocidos en el estado del arte: Inception-v3, ResNet-50,
Inception-ResNet-v2 y DenseNet-201, para distinguir entre diferentes enfermedades de la piel, después de
realizar la implementación de
los clasificadores International Skin Imaging Collaboration (ISIC) y CIIU, en los años 2016 y 2017 lograron
concluir que el clasificador
que mejor se desempeño fue el ResNet-50, arrojando resultados de 81.57% y 89.28% en las dos ISIC aplicadas.
Multiple skin lesions diagnostics via
integrated deep convolutional networks for segmentation and classification. Computer Methods and
Programs in Biomedicine, 190, 105351. https://doi.org/10.1016/j.cmpb.2020.105351.
Por otro lado, y teniendo en cuenta el aumento drástico en la tasa de fatalidades por cancel de piel dadas las variedades de la sintomatología, confirma que la detección temprana en la etapa prematura es necesaria para prevenir la propagación del cáncer. Por ejemplo, Krishna Monika et al.
(Krishna Monika et al., 2020)
narra la creación de un proyecto que trata sobre la detección y clasificación de varios tipos de cáncer de
piel utilizando
herramientas de procesamiento de imágenes y aprendizaje automático. En la etapa de preprocesamiento, las
imágenes dermatoscópicas se consideran como entrada.
El método de la maquinilla de afeitar sin filo se utiliza para eliminar todas las partículas de pelo no
deseadas en la lesión de la piel,
luego se utiliza el filtro gaussiano para suavizar la imagen. Para filtrar el ruido y preservar los bordes
de la lesión se utiliza un filtro
de mediana. Dado que el color es una característica importante en el análisis del tipo de cáncer, la
agrupación de k-medias basada en el color
se realiza en la fase de segmentación.
Skin cancer detection and
classification using machine learning. Materials Today: Proceedings, 33, 4266–4270. https://doi.org/10.1016/J.MATPR.2020.07.366.
4. RESULTADOS
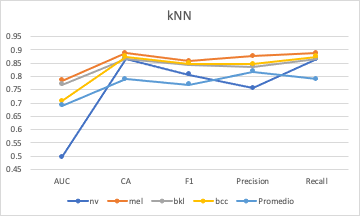
En el proceso de implementación de la muestra, se realiza por medio de python, utilizando una muestra de 115 imágenes, de estas se usaron 100 de entrenamiento y 15 de test, este procedimiento se realiza duplicando el número de imágenes de entrenamiento al igual que las de test, pasando por 200, 400 y 800 imágenes de entrenamiento y 30, 60, 120 imágenes de test, para cada uno de los tipos de cáncer manualmente etiquetados que cuentan con la cantidad de imágenes para pertenecer a cada grupo, que tiene la data mencionada, en este proceso se realiza de manera controlada sobre la detección de cáncer de piel.En este proceso se aplican kNN, SVM, TREE, Neural Network, cuyos resultados de predicción se complementan con el resultado del análisis de AUC, AC y predicted el modelo de la fig.3, para poder analizar correctamente se realiza para la implementación de las 200 y 400 imágenes de entrenamiento (train) y 30 y 60 imágenes de prueba (test), obteniendo buenos resultados pese a resultados tienen una gran variación, obteniendo los mejores resultados de manera inicial al aplicar el modelo de maquina de soporte vectorial SVM, en donde se puede visualizar en la fig 4, el resultado más alto de predicción lo tiene el melanoma (mel).

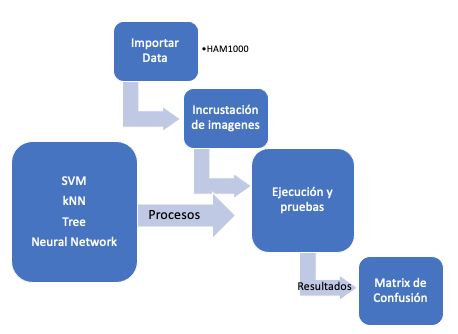
Fig. 3 Implementación del modelo de aprendizaje.
Fuente: autor
Fuente: autor
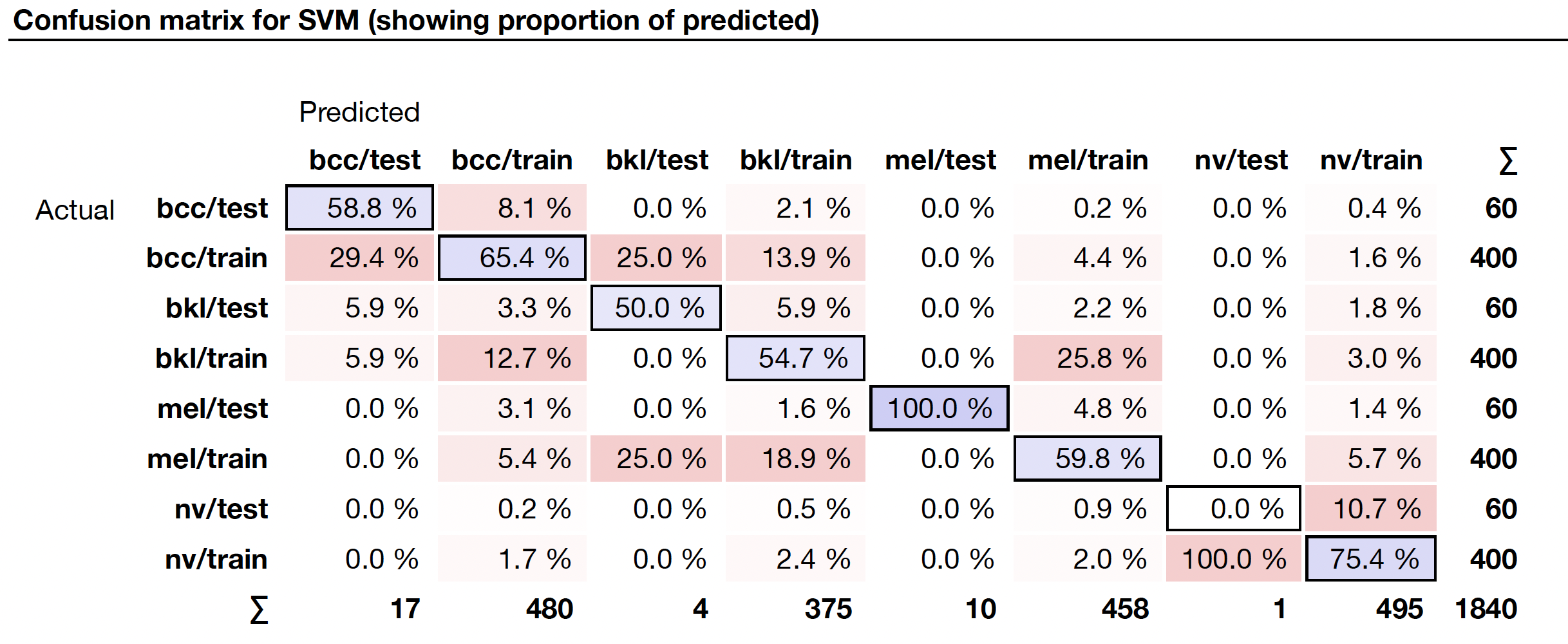
En este procedimiento se encuentra en la ejecución del segundo grupo de imágenes correspondientes a las 400 imágenes un mayor desempeño en el SVN, arrojando predicciones de hasta el 100% en la ejecución de test and score, para el modelo de la máquina de soporte vectorial SVM. Si bien se presentan resultados de 100% en la ejecución, estos resultados varían acorde a las muestras implementadas y el tipo de muestra seleccionada, esto permite ajustar las fórmulas para encontrar una precisión en constante mejora, y que la variación entre las muestras no afecte los altos porcentajes de predicción calculados.


Fig. 4 kNN ejecutado para 4 tipos de cáncer.
Fuente: Autor.
Fuente: Autor.
5. CONCLUSIONES
La generación de nuevo conocimiento, por medio de la exploración de la historia escrita o recopilada por otros investigadores, facilita y orienta de una mejor manera la evolución de los saberes, de los procesos experimentales y de la mejora en los procesos ya probados, permitiendo a los nuevos investigadores a construir sobre cimientos y fortalecer de la mejor manera la construcción de nuevas herramientas para el saber, es por ello que la recopilación de implementaciones de inteligencia artificial en el sector salud, y de manera más específica, la implementación en el cáncer de piel, abre las puertas a una investigación con bases para mejorar y/o complementar los trabajos ya realizados.Esta implementación permitió poder tener de manera sólida una descripción de apoyo a la aplicación de herramientas para verificar la predicción que se genera en la implementación de modelos de inteligencia artificial, generando predicciones que permiten clasificar con un alto grado de precisión, que permita detectar si, las muestras escogidas hacen parte de un cáncer de piel o no, de esta forma brindarle al dermatólogo o al oncólogo tener un primer análisis de las muestras analizadas.
6. REFERENCIAS
Abdul Hamid, D. S. Bin, Goyal, S. B., & Bedi, P. (2021). Integration of Deep Learning for Improved Diagnosis of Depression using EEG and Facial Features. Materials Today: Proceedings. https://doi.org/10.1016/J.MATPR.2021.05.659Al-masni, M. A., Kim, D., & Kim, T. (2020). Computer Methods and Programs in Biomedicine Multiple skin lesions diagnostics via integrated deep convolutional networks for segmentation and classification. Computer Methods and Programs in Biomedicine, 190, 105351. https://doi.org/10.1016/j.cmpb.2020.105351
Daneshjou, R., He, B., Ouyang, D., & Zou, J. Y. (2021). How to evaluate deep learning for cancer diagnostics – factors and recommendations. Biochimica et Biophysica Acta (BBA) - Reviews on Cancer, 1875(2), 188515. https://doi.org/10.1016/J.BBCAN.2021.188515
Deng, L., & Yu, D. (2019). Deep Learning Methods and Applications. SpringerBriefs in Computer Science, 31–42. https://doi.org/10.1007/978-981-13-3459-7_3
Dorado-Díaz, P. I., Sampedro-Gómez, J., Vicente-Palacios, V., & Sánchez, P. L. (2019). Applications of Artificial Intelligence in Cardiology. The Future is Already Here. In Revista Espanola de Cardiologia (Vol. 72, Issue 12, pp. 1065–1075). Elsevier Doyma. https://doi.org/10.1016/j.recesp.2019.05.016
Fontecha Pardo, N. A., Quiroga Sarmiento, J. S., nicolas.fontechap@campusucc.edu.co, & juan.quirogas@campusucc.edu.co. (2020). Implementación de algoritmos de inteligencia artificial enfocados en el análisis de los trastornos del estado de ánimo para prevenir futuros suicidios por medio de la red social Facebook. Aprendeia. (22 de 11 de 2020). Obtenido de Https://Aprendeia.Com/Naive-Bayes-Teoria-Machine-Learning/.
Garay, N., Abascal, J., & Gardeazabal, L. (2002). Mediación emocional aplicada en sistemas de comunicación aumentativa y alternativa. Inteligencia Artificial, 6(16). https://doi.org/10.4114/ia.v6i16.743
Gómez Rivas, J., Toribio Vázquez, C., Ballesteros Ruiz, C., Taratkin, M., Marenco, J. L., Cacciamani, G. E., Checcucci, E., Okhunov, Z., Enikeev, D., Esperto, F., Grossmann, R., Somani, B., & Veneziano, D. (2021). Inteligencia artificial y simulación en urología. Actas Urológicas Españolas. https://doi.org/10.1016/J.ACURO.2020.10.012
Han, S. S., Park, I., Chang, S. E., Lim, W., & Kim, M. S. (2020). Augmented Intelligence Dermatology : Deep Neural Networks Empower Medical Professionals in Diagnosing Skin Cancer and Predicting Treatment Options for 134 Skin Disorders. Journal of Investigative Dermatology, 140(9), 1753–1761. https://doi.org/10.1016/j.jid.2020.01.019
Hekler, A., Utikal, J. S., Enk, A. H., Hauschild, A., Weichenthal, M., Maron, R. C., Berking, C., Haferkamp, S., Klode, J., Schadendorf, D., Schilling, B., Holland-Letz, T., Izar, B., von Kalle, C., Fröhling, S., Brinker, T. J., Schmitt, L., Peitsch, W. K., Hoffmann, F., … Thiem, A. (2019). Superior skin cancer classification by the combination of human and artificial intelligence. European Journal of Cancer, 120, 114–121. https://doi.org/10.1016/J.EJCA.2019.07.019
Hernández, J. C. (2020). PROBLEMAS ÉTICO-JURÍDICOS DE LAS DECISIONES ALGORÍTMICAS Y EL BIG DATA * Joslay Polanco Medina.
Jofre, M., & Abeldaño, A. (2021). Artificial intelligence: Will replace the dermatologist making diagnoses? Piel, 36(5), 331–335. https://doi.org/10.1016/j.piel.2020.06.003
Koh, J., Yoon, Y., Kim, S., Han, K., & Kim, E. K. (2021). Deep Learning for the Detection of Breast Cancers on Chest Computed Tomography. Clinical Breast Cancer. https://doi.org/10.1016/J.CLBC.2021.04.015
Krishna Monika, M., Arun Vignesh, N., Usha Kumari, C., Kumar, M. N. V. S. S., & Laxmi Lydia, E. (2020). Skin cancer detection and classification using machine learning. Materials Today: Proceedings, 33, 4266–4270. https://doi.org/10.1016/J.MATPR.2020.07.366
Leiva Vazquez, M., Gonzalez Benitez, N., Hechavarria Hernandez, J., Rivero Peña, Y., & Daher Nader, J. E. (2018). El diagnóstico de enfermedades desde el Análisis Inteligente de los Datos.
Maisueche Cuadrado, A. (2019). Utilización Del Machine Learning En La Industria 4.0.
McClendon, L., & Meghanathan, N. (2015). Using Machine Learning Algorithms to Analyze Crime Data. Machine Learning and Applications: An International Journal, 2(1), 1–12. https://doi.org/10.5121/mlaij.2015.2101
Mitchel, T. M. (2017). Machine Learning. In Proceedings of the International Conference on Document Analysis and Recognition, ICDAR. https://doi.org/10.1109/ICDAR.2019.00014
Organización Mundial de La Salud, O. (2021). Cáncer. WHO.
P, T., C, R., & H, K. (2018). The HAM10000 dataset, a large collection of multi-source dermatoscopic images of common pigmented skin lesions. Scientific Data, 5. https://doi.org/10.1038/SDATA.2018.161
Russel, S., & Norvig, P. (2010). Artificial intelligence, A Modern Approach. In 2010 The 2nd International Conference on Computer and Automation Engineering, ICCAE 2010 (Vol. 4). https://doi.org/10.1109/ICCAE.2010.5451578
Saravanan, S., Heshma, B., Shanofer, A. V. A., & Vanithamani, R. (2020). Skin cancer detection using dermoscope images. Materials Today: Proceedings, xxxx. https://doi.org/10.1016/j.matpr.2020.08.388
Yan, T., Zhang, L., & Peng, C. (2019). Intelligent skin cancer diagnosis using improved particle swarm optimization and deep learning models. Applied Soft Computing Journal, 84, 105725. https://doi.org/10.1016/j.asoc.2019.105725
Yin, S., Peng, Q., Li, H., Zhang, Z., You, X., Fischer, K., Furth, S. L., Fan, Y., & Tasian, G. E. (2020). Multi-instance Deep Learning of Ultrasound Imaging Data for Pattern Classification of Congenital Abnormalities of the Kidney and Urinary Tract in Children. Urology, 142, 183–189. https://doi.org/10.1016/J.UROLOGY.2020.05.019